Цветные металлы — особый класс нержавеющих металлов и сплавов, в составе которых нет железа. Сюда входят олово, медь, цинк, никель, серебро, золото. Металлы называются цветными, потому что каждый из них имеет определенный окрас. Они отличаются прочностью и долговечностью, поскольку формируют на своей поверхности защитную оксидную пленку и проявляют устойчивость к негативным факторам внешней среды.
В начале XX века насчитывалось около 20 наименований нежелезных металлов, а сегодня их количество уже превышает 70. Добычей, обогащением руд и выплавкой таких материалов занимается цветная металлургия. Способ производства — высокотемпературная плавка. За каждым изделием стоит долгая и кропотливая работа — металлы подвергаются механической обработке и проходят через ковку, сварку, прессование, штамповку, грунтование и прочие процессы.
Свойства
Цветные металлы обладают высокой тепло– и электропроводностью, коррозионной стойкостью, стабильностью в температурном диапазоне и инертностью к воздействию агрессивной среды. В отличие от железа, они не реагируют на влагу и кислород, растворяют газы при нагревании (кроме интертных) и с легкостью взаимодействуют с ними.
Группы
Ученые подразделяют цветные металлы на несколько групп:
- Тяжелые. Олово, медь, никель, цинк, свинец и т.п. Добываются из сульфидных и окисленных полиметаллических руд. Мировое производство металлов данной категории достигает нескольких миллионов тонн в год.
- Легкие. Алюминий, титан, магний, натрий, калий, кальций, бериллий, стронций, барий и другие элементы этой группы имеют самую низкую удельную массу среди остальных нежелезных металлов.
- Благородные. Золото, серебро, платина, рутений, родий, палладий, осмий и иридий входят в число редких драгоценных металлов и отличаются повышенной стойкостью к окислению и коррозии.
- Малые. Представители группы — ртуть, кобальт, мышьяк, сурьма, висмут и т.п. Добываются в небольшом количестве вместе с тяжелыми металлами.
- Тугоплавкие. Известны как самые износостойкие металлы. К ним относится цирконий, ванадий, хром, вольфрам, молибден и другие элементы с высокой плотностью и температурой плавления.
- Редкоземельные. Представлены 17 металлами серебристо–белого цвета: гольмий, тулий, скандий, самарий, европий, диспрозий, лютеций, прометий и т.д. Обладают одинаковыми химическими свойствами.
Применение
В последние годы спрос на цветные металлы резко увеличился. Они влияют на развитие многих отраслей промышленности и широко применяются в авиа– и машиностроении, радиоэлектронике, ракетной и атомной технике, сфере высоких технологий, а также в быту.
Нежелезные металлы — незаменимое сырье в производстве металлопроката, крупных конструкций и небольших изделий.
Вы можете заказать цветные металлы и сплавы на нашем сайте. На странице каталога представлен широкий ассортимент товаров с подробным описанием и ценами. Стоимость за 1 кг зависит от вида материала и варьируется от 135 до 2200 рублей. Денежные средства принимаем на расчетный счет. Подробнее об условиях покупки цветного металла в Москве и регионах России читайте здесь.
Алюминий. В земной коре содержится примерно 8, 8 % алюминия, что в 1, 7 раза превышает содержание железа (5, 1 % [371]). Алюминий самый распространенный цветной металл как по содержанию в земной коре, так и по объему производства и масштабам применения.
Алюминий не претерпевает полиморфных превращений. Во всем температурном интервале вплоть до точки плавления он имеет кристаллическую решетку гранецентрированного куба (см. табл. 1. 2). Плотность алюминия в твердом и жидком состояниях уменьшается с повышением его чистоты и температуры. Плотность жидкого алюминия связана с температурой зависимостью [260]
у = 2,385 — 2,8•10 (Т — Тал), г/см 3 ,
где величина 2,385 представляет собой плотность жидкого алюминия при Тпл (933 К).
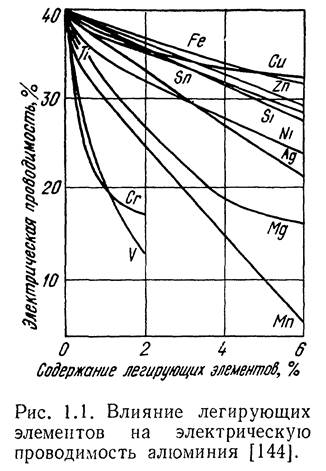 |
Алюминий весьма пластичен, хорошо сваривается, легко поддается всем видам обработки давлением, а также резанию, хороший проводник тепла и электричества. Электрическая проводимость алюминия составляет 60 — 65% электрической проводимости меди. Поскольку алюминий примерно в три раза легче меди, алюминиевый провод с таким же электросопротивлением легче, чем медный. Примеси и легирующие элементы уменьшают электрическую проводимость алюминия (рис. 1. 1). Алюминий слабопарамагнитен. При Т= 1,2 К переходит в сверхпроводящее состояние [370].
Алюминий обладает специфическим свойством, определившим его применение в атомных реакторах, — способностью поглощать нейтроны. Известно, что чем ниже поперечное сечение поглощения тепловых нейтронов, измеряемое в барнах (16= 10- 24 см 2 ), тем выше поглощающая способность металла. Этот показатель у алюминия значительно ниже (0, 215 б), чем у других конструкционных металлов, таких, как железо (2, 43 б), медь (3, 59 б) и никель (4, 5 б) [384].
Во всех стойких соединениях алюминий проявляет степень окисления +3, однако при высоких температурах, главным образом в газообразных соединениях, он проявляет и другие степени окисления. При этом образуются так называемые субсоединения: А1О, АlO2, А12О и др.
Алюминий — химически активный металл. Даже при нормальной температуре на его поверхности образуется оксид А12О3. Наличие оксидной пленки на поверхности алюминия предохраняет его от дальнейшего взаимодействия с окружающей средой. Тугоплавкая оксидная пленка затрудняет процесс сварки алюминия. Литейные свойства алюминия невысоки из-за большой усадки малой жидкотекучести металла и высокой пористости получаемого литья.
Благодаря защитному действию оксидной пленки алюминий и его сплавы обладают высокой коррозионной стойкостью в атмосферных условиях и в тех средах, которые не разрушают пленку. Сероводород, сернистый газ и аммиак не влияют на коррозионную стойкость алюминия при комнатной температуре, а пар, дистиллированная и чистая пресная вода — и при высокой температуре. Алюминий обладает высокой коррозионной стойкостью в морской воде, которая, однако, понижается при его контакте с углеродистой и нержавеющей сталями. Это объясняется тем, что углеродистая сталь находится в III, а нержавеющая хромоникелевая сталь — в IV группе но значениям электродных потенциалов. Поскольку алюминий принадлежит ко II группе, происходит его более интенсивная контактная коррозия.
Алюминий достаточно устойчив в концентрированной азотной кислоте, в 100%-ной серной кислоте и в ее растворах концентрацией до 10 %. С повышением температуры раствора и концентрации кислоты коррозия резко возрастет. Сильнее действуют на алюминий соляная кислота, едкие щелочи (NaOH, КОИ), которые интенсивно растворяют алюминий с образованием алюминатов (NaA102, КАЮ2). В контакте с большинством металлов алюминий является анодом, поэтому коррозия его в электролитах ускоряется.
Алюминиевые сплавы делят на деформируемые и литейные, на термически неупрочняемые и термически упрочняемые.
К деформируемым относится и технический алюминий.
Технически чистый алюминий содержит ряд примесей. Допускаемое их количество в алюминии, выпускаемом промышленностью, приведено в табл. 1. 5. Помимо указанных алюминий технической чистоты содержит и ряд других неконтролируемых примесей (табл, 1.6) [173). Электросопротивление и механические свойства деформированного технического алюминия в значительной мере определяются чистотой металла (табл. 1.7). Наиболее распространенные марки и основные механические свойства листов из технически чистого алюминия приведены в табл. 1.8. Из него изготавливают также проволоку, прутки, профили и другие полуфабрикаты.
Холодная пластическая деформация заметно повышает прочность и снижает пластичность металла. Например, нагартовка листов технического алюминия повышает его предел прочности до 147—176 МПа. При этом относительное удлинение снижается до 1—2 % [173]. Упрочнение, достигнутое в результате нагартовки, сохраняется при нагревах до температур ниже температуры рекристаллизации (для алюминия марки А995 примерно 400 °С)
Большая склонность к росту зерна — отличительная особенность алюминия, которую необходимо учитывать при сварке и горячей обработке. Размер зерна в алюминии и его сплавах можно регулировать рекристаллизационным отжигом. Величина зерна после рекристаллизации зависит (как и у других металлов) от степени предшествующей пластической деформации (рис. 1. 2) и во многом определяет свойства алюминия после отжига [144]. Температуру рекристаллизационного отжига выбирают в интервале 300—500 °С при выдержке 0, 5—2 ч (144, 146]. Скорость охлаждения технического алюминия не влияет па конечную структуру металла, и ее можно выбирать произвольно. Обычно охлаждение полуфабрикатов производят на воздухе [146].
Относительно малый атомный радиус алюминия является причиной того, что алюминий образует с другими элементами ограниченные твердые растворы (цинк, магний, литий) и интерметаллиды (марганец, железо, медь и др. ). Поэтому даже незначительное количество неизбежных примесей в алюминии — железа и кремния — существенно влияет на структуру и свойства металла. Наличие этих примесей способствует измельчению зерна в техническом алюминии и определяет уровень его механических свойств. Так, если предел прочности алюминия марки А999 составляет примерно 39, 7 МПа, то в алюминии марки А7 (Fe
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Учись учиться, не учась! 10468 — 

— тяжёлые металлы — медь, никель, цинк, свинец, олово;
— лёгкие металлы — алюминий, магний, титан, бериллий, кальций, стронций, барий, литий, натрий, калий, рубидий, цезий;
— благородные металлы — золото, серебро, платина, осмий, рутений, родий, палладий;
— малые металлы — кобальт, кадмий, сурьма, висмут, ртуть, мышьяк;
— тугоплавкие металлы — вольфрам, молибден, ванадий, тантал, ниобий, хром, марганец, цирконий;
— редкоземельные металлы — лантан, церий, празеодим, неодим, самарий, европий, гадолиний, тербий, иттербий, диспрозий, гольмий, эрбий, тулий, лютеций, прометий, скандий, иттрий;
— рассеянные металлы — индий, германий, таллий, таллий, рений, гафний, селен, теллур;