Почему одни атомы могут иметь только одну валентность, а другие — несколько? Для ответа на этот вопрос обратимся к квантово-механической модели строения атома, согласно которой, электроны вокруг атомного ядра располагаются на, так называемых, энергетических уровнях (см. Электронная структура атомов).
Как известно, атомы могут вступать в химические реакции с другими атомами, с образованием химических связей, путем отдачи/принятия своих/чужих электронов, которые называются валентными (см. Валентность).
В Периодической таблице химических элементов Д. И. Менделеева все атомы отображены в их основном состоянии (состоянии с минимальной энергией). Основное состояние атома описывается электронной конфигурацией атома, согласно его положению в Периодической таблице (см. Таблицу электронных конфигураций атомов химических элементов по периодам.
В определенных ситуациях, некоторые атомы, получая энергию извне, переходят в, так называемое, возбужденное состояние, в котором пребывают относительно короткое время, поскольку возбужденное состояние является нестабильным, после чего возбужденный атом отдает энергию и возвращается в свое основное (стабильное) состояние.
Рассмотрим основное и возбужденное состояние атома на конкретных примерах.
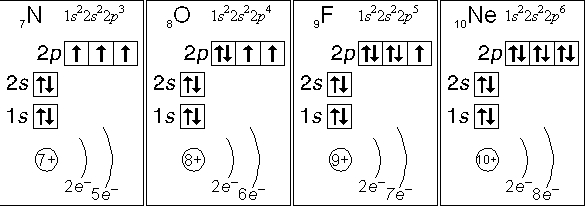
Рис. Электронные конфигурации атомов азота, кислорода, фтора, неона.
- атом азота (N):
- кол-во неспаренных электронов: 3
- ковалентность: 3
Азот, кислород, фтор и неон не могут иметь возбужденного состояния по той простой причине, что они не имеют свободной орбитали с более высокой энергией, на которую могли бы "перескакивать" спаренные электроны с орбиталей с меньшей энергией.
Рассмотрим атом серы, который находится в одной с кислородом группе — 16 (VIa), но, в отличие от кислорода, у атома серы имеется свободная d-орбиталь, существенно расширяющая валентные возможности элемента:
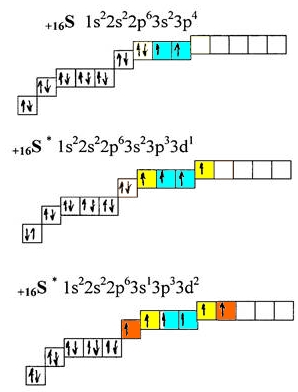
Рис. Возбужденное состояние атома серы.
В основном состоянии атом серы имеет 2 валентных электрона (голубой цвет). Как видно из вышеприведенного рисунка, получая энергию извне, у атома серы могут появляться еще 2 (желтый цвет) или 4 (желтый+оранжевый) дополнительных валентных электрона, при этом общее кол-во валентных электронов увеличивается до 4 или 6 соответственно.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Возбужденное состояние — молекула
Возбужденные состояния молекул , в которые они переходят при поглощении квантов света, также являются синглетными, так как в процессе возбуждения спин молекулы не изменяется. Однако после возбуждения молекул, имеющих тг-электроны ( или rf — электроны, / электроны с я-симметрией), может произойти обращение спина электрона. [1]
Возбужденные состояния молекул иногда разрушаются за счет переноса большого количества энергии к другим частицам в системе. Частицы-акцепторы в этом процессе сами переходят в возбужденное состояние. [2]
Возбужденное состояние молекулы азота N2 является ме-тастабильным и отстоит от основного уровня на расстоянии 2318 см 1, что весьма близко к энергетическому уровню ( 001) молекулы СОа. Ввиду метастабильности возбужденного состояния Na при прохождении тока число возбужденных атомов накапливается. При столкновении N2 с ССЬ происходит резонансная передача энергии возбуждения от N2 к СОа. Обычно для уменьшения заселенности уровня ( 100), который имеет большое время жизни, что ухудшает генерацию при переходе на этот уровень, добавляют гелий. [3]
Возбужденные состояния молекул хлорофилла должны играть важную роль в процессе фотосинтеза. Поэтому много работ было посвящено вопросу о том, каким образом вообще могут реагировать молекулы хлорофилла и порфириноподобные молекулы. Некоторые результаты таких исследований заставляют предположить, что важной промежуточной ступенью этих реакций может служить образование триплетного состояния. [4]
Известные возбужденные состояния молекул галогенидов щелочных металлов являются нестабильными состояниями или состояниями, в которых кривая потенциальной энергии молекулы имеет неглубокий минимум, поэтому они не рассматриваются в настоящем Справочнике. [5]
В возбужденном состоянии молекулы или атомы, как правило, находятся короткое время ( Ю-9-10-8 с); затем электроны самопроизвольно ( спонтанно) переходят на более низкий энергетический уровень или на уровень основного состояния. Этот процесс сопровождается выделением энергии в виде тепла или электромагнитного излучения, или одновременно того и другого. [6]
В принципе любое возбужденное состояние молекулы может быть материнским для рассматриваемых резонансных состояний. [7]
Если энергии возбужденных состояний молекул Л и D точно одинаковы, то два состояния, описываемые волновыми функциями Ч о 1 А и TD A, при наличии подходящего взаимодействия являются вырожденными. Из нестационарной теории возмущений следует, что при таких условиях имеется определенная вероятность передачи энергии от одного из вырожденных состояний к другому. Эта вероятность увеличивается во времени и уменьшается в пространстве пропорционально шестой степени расстояния между центрами двух взаимодействующих молекул. [8]
Время существования возбужденного состояния молекулы , вызванного электронным переходом, уже допускает рассеяние энергии по вращательным и колебательным уровням. [9]
Время жизни возбужденного состояния молекулы на верхних электронных уровнях относительно мало. Возбужденная молекула в конечном итоге возвращается в основное состояние. При этом переходе выделяется энергия в виде излучения ( флуоресценция или фосфоресценция) или тепла. Факторы, определяющие тип распада, еще точно не известны. [11]
Важность такого возбужденного состояния молекулы в фотохимии оправдывает введение для него специального термина. Мы будем пользоваться термином фото-активированные молекулы или молекулярные состояния в этом особом смысле, чтобы отличить эти состояния от обычных возбужденных молекул с коротким временем жизни, которые имеют меньшее фотохимическое значение. [12]
Точное описание возбужденного состояния молекул может почти всегда включать определенную СТ-составляющую. [13]
Потенциальная кривая возбужденного состояния молекулы не имеет минимума. В этом случае в спектрах в газовой фазе нет линейчатого поглощения, так как возбужденное состояние не имеет дискретных колебательных уровней. [15]
Эксимерные лазеры.
В качестве активной среды в лазерах этого типа выступают молекулы, которые могут существовать только в возбужденном состоянии. Такие молекулы называются эксимерами. В эксимерных молекулах для лазерной генерации используются электронно-колебательные переходы между устойчивым возбужденным (Еи химически неустойчивым основным состоянием (Е0). В качестве примера эксимерных молекул можно привести возбужденные молекулы благородных газов и их соединения: Хе£ , Кг2 , Аг2 , ХеГ*, ХеСГ, КгЕ Аг1Г* и т. д. (звездочка означает возбужденную молекулу).
Если в рабочем объеме создать большую концентрацию эксимерных молекул, например, пучком электронов с энергией до 1 МэВ и плотностью тока до 10 11 А/см 2 , то может быть получена инверсная населенность возбужденного уровня Ег. В результате возникает инверсия населенностей на переходах между верхним связанным состоянием Е, и нижним неустойчивым состоянием Е0. Из-за того, что верхнее состояние Е, представляет собой полосу электронно-колебательных уровней, а в нижнем состоянии отсутствует дискретная вращательно-колебательная структура уровней энергии, излучение эксимерного лазера происходит в сравнительно широком спектральном диапазоне, что позволяет перестраивать частоту генерации в пределах этого перехода.
Помимо широкополосности излучения, можно отметить также то, что эксимерные переходы из возбужденного в неустойчивое основное состояние из-за быстрой диссоциации эксимерной молекулы сопровождаются практически мгновенным опустошением нижнего лазерного уровня. Время жизни экси- меров мало (
9 . Ю 8 с), поэтому эксимерные лазеры работают в основном в импульсном режиме, генерируя короткие импульсы излучения с энергией до 10 Г) Дж и КПД до 10%. Эксимерные лазеры излучают энергию в УФ диапазоне длин волн (
Химические лазеры.
Инверсия населенностей в химических лазерах достигается за счет энергии химических реакций между отдельными составляющими активной среды, при этом используются только экзотермические реакции. В результате этих реакций в газовых смесях, например, таких, как НЕ, происходит выделение энергии, большая часть которой переходит в колебательную энергию молекул.
Таким образом, основным достоинством химических лазеров является прямое преобразование химической энергии в энергию электромагнитного лазерного излучения с высоким КПД (
10%). К другим достоинствам химических лазеров можно отнести большие мощности излучения в непрерывном режиме (> 10 кВт), высокое значение удельной энергии (
10 Дж/л), отсутствие громоздких источников питания. Химические лазеры работают на колебательно-вращательных уровнях в спектральном диапазоне 3. 10 мкм.
Рентгеновские лазеры (X 3 , что затрудняет генерацию индуцированного излучения (см. п. 17.1).
В качестве активных сред в рентгеновских лазерах используются плазменные среды с многократно ионизированными атомами. Энергетические состояния ионов по своей структуре аналогичны энергетической структуре соответствующих атомов с той лишь разницей, что значения разности энергий уровней ионизированных атомов намного больше, чем для нейтральных. Например, спектры разрешенных значений энергии восьмикратно ионизированного атома аргона Аг 8+ или иона селена Эе 24 * аналогичны спектру атома N6, но значения разности энергий уровней у этих многократно ионизированных атомов Аг и Эе больше, чем у Ке, в 50 и 500 раз соответственно.
Получение плазмы с такими многократно ионизированными (многозарядными) ионами возможно только в установках типа тех, которые используются для термоядерного синтеза, поэтому это ограничивает их применение в настоящее время. Однако в силу важности отмеченных выше возможных применений, работы по созданию этих лазеров в развитых странах проводятся достаточно интенсивно. В настоящее время уже получена лазерная генерация в режиме сверхкоротких импульсов на Эе 24 *,
Аг 8 % А^ 7+ и ряде других элементов в диапазоне длин волн от 3 до 50 нм.
Лазеры на свободных электронах.
В лазерах этого типа используются основные преимущества электронных вакуумных приборов с динамическим управлением, например, ЛБВО и ЛБВМ (см. гл. 13, 14). В лазерах на свободных электронах активной средой являются электронные потоки, ускоренные до релятивистских скоростей и движущиеся через ондулятор. Ондулятор представляет устройство с периодически изменяющимся в пространстве электрическим или магнитным полем. В магнитном ондуляторе поле формируется набором расположенных друг за другом магнитов с чередующейся полярностью. Кроме поступательного движения, электроны под действием такого магнитного поля совершают периодические колебания (осцилляции), которые сопровождаются электромагнитным излучением с частотой оо()
ц/А,, где и — скорость переносного (продольного) движения электронов, О = X — пространственный период изменения магнитного ПОЛЯ.
Расчеты показывают, что для получения излучения электронов в видимом диапазоне спектра необходимо разогнать их до энергии в 50 МэВ (при 2) = 1 см). Современные ускорители заряженных частиц позволяют разогнать электроны до энергий, превышающих 500 МэВ, что будет соответствовать излучению на красном краю рентгеновского диапазона.